
14 Mar Epidemiologia de la epilepsia
La epilepsia es una de las enfermedades neurológicas más comunes y afecta a personas de todas las edades, razas, clases sociales y ubicaciones geográficas. La epilepsia es una enfermedad del cerebro caracterizada por una predisposición duradera a generar convulsiones y por las consecuencias neurobiológicas, cognitivas, psicológicas y sociales de las recurrencias de las convulsiones. Las crisis epilépticas son eventos paroxísticos recurrentes caracterizados por alteraciones conductuales estereotipadas que reflejan los mecanismos neurales subyacentes de la enfermedad. El diagnóstico diferencial de la epilepsia abarca una serie de condiciones clínicas caracterizadas por una alteración transitoria de la conciencia y/o del comportamiento. En la mayoría de los casos, la enfermedad se puede diagnosticar a través de una historia cuidadosa o mediante la observación de una convulsión. Aunque se puede identificar un agente etiológico, todavía en aproximadamente la mitad de los casos, la causa se desconoce. Una predisposición genética variable a manifestar convulsiones y la diferente distribución de algunos factores de riesgo ambientales pueden explicar la heterogeneidad de la frecuencia, curso y consecuencias de la enfermedad en el mundo. Además de la recurrencia de las convulsiones, la causa subyacente y los efectos adversos del tratamiento tienen consecuencias neurológicas, cognitivas, psicológicas y sociales que afectan significativamente la calidad de vida de los afectados y hacen de la enfermedad una entidad nosográfica compleja.1
La epileptogénesis es el proceso de convertir un cerebro no epiléptico en uno capaz de generar convulsiones espontáneas y recurrentes. El proceso se conceptualiza como el resultado de un desequilibrio entre la actividad excitatoria e inhibidora dentro de una red neuronal, de modo que es probable que funcione de manera excesiva, oscilatoria, hipersincrónica, que cuando se mantiene, interrumpe el procesamiento neuronal normal y es capaz de interrumpir otras redes neuronales. Para las epilepsias focales, las redes involucran circuitos neuronales en un hemisferio, comúnmente límbico o neocortical. El desequilibrio entre excitación e inhibición que da como resultado redes epileptogénicas no es necesariamente solo un aumento de excitación o una pérdida de inhibición; un aumento anómalo de la inhibición también puede ser proepiléptico en algunas circunstancias, como las crisis de ausencia o las epilepsias límbicas en el cerebro inmaduro. Se cree que la mayoría de las epilepsias generalizadas tienen una base genética. Por el contrario, se pensaba que las epilepsias focales se debían principalmente a anomalías cerebrales estructurales, en particular en la epilepsia resistente a los medicamentos. Sin embargo, se ha encontrado un número creciente de mutaciones genéticas heredadas y de novo en la epilepsia focal no lesional.2
Se han encontrado más de 30 genes mutados en familias con epilepsias monogénicas autosómicas dominantes raras con alta penetrancia. Las mutaciones iniciales descubiertas estaban principalmente en genes que codifican canales iónicos; sin embargo, se han encontrado varias mutaciones en genes de canales no iónicos, incluidos genes para receptores neuronales, factores de transcripción y enzimas. Las personas con epilepsias monogénicas familiares representan un pequeño porcentaje (5 a 10 %) de todas las epilepsias genéticas. Las causas subyacentes de la mayoría de los casos de presuntas epilepsias genéticas generalizadas, como la epilepsia mioclónica juvenil, aún se desconocen a pesar de las investigaciones intensivas. Es probable que la causa genética de estas epilepsias comunes sea compleja e involucre contribuciones de múltiples genes, ya sea dentro de los individuos o entre diferentes individuos con el mismo síndrome.2
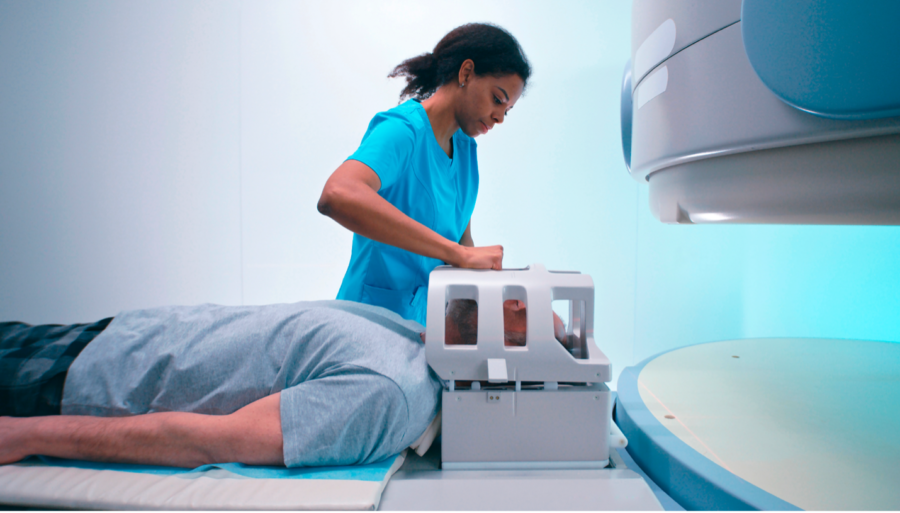
La resonancia magnética (RM) es la herramienta de diagnóstico por imágenes estándar y muestra lesiones epileptógenas en aproximadamente el 20 % de las personas con epilepsia recién diagnosticada y en más de la mitad de las personas con epilepsia focal resistente a los medicamentos. En comparación con aquellos sin una lesión en la RM, las personas en las que se detecta una lesión en la RM tienen un mayor riesgo de recurrencia después de una primera convulsión o de continuar teniendo convulsiones después del tratamiento. La RM debe realizarse con un protocolo adecuado para la epilepsia que comprenda al menos 1 mm tridimensional volumétrico ponderado en T1, axial y coronal ponderado en T2 y secuencias de recuperación de inversión atenuada por líquido (incluida la angulación del hipocampo) y hemosiderina axial o secuencias T2 sensibles a la calcificación o secuencias ponderadas de susceptibilidad. La evaluación de un experto probablemente sea igualmente importante ya que, de lo contrario, se pueden pasar por alto algunas lesiones sutiles, como la esclerosis del hipocampo o la displasia cortical focal. En personas con epilepsia focal resistente a los medicamentos con resonancias magnéticas previas aparentemente normales, a menudo vale la pena volver a escanear con un escáner o secuencias diferentes (figura 1).2
En conclusión, la epilepsia es una enfermedad de síntomas complejos con múltiples factores de riesgo y en muchos casos tiene una fuerte predisposición genética, más que una condición con una sola expresión y una sola causa. Los avances en tecnología genómica están comenzando a mostrar la compleja arquitectura genética de las epilepsias. Las comorbilidades se reconocen cada vez más como importantes marcadores etiológicos y pronósticos. Los medicamentos anticonvulsivos suprimen las convulsiones en hasta dos tercios, si no más, de todos los individuos, pero no alteran el pronóstico a largo plazo. La epilepsia es una carga importante en términos de calidad de vida, morbilidad y riesgo de mortalidad prematura, especialmente en aquellos que continúan teniendo convulsiones. La cirugía de epilepsia es la forma más efectiva de lograr la ausencia de convulsiones a largo plazo, pero es una opción solo para algunas personas con epilepsia resistente a los medicamentos. Con una mejor comprensión de la epileptogénesis, los determinantes epigenéticos y la farmacogenómica surge la esperanza de mejores tratamientos farmacológicos y no farmacológicos curativos y modificadores de la enfermedad.2
Referencias:
- Beghi E. The Epidemiology of Epilepsy. Neuroepidemiology. 2020;54(2):185-191. doi: 10.1159/000503831. Epub 2019 Dec 18. PMID: 31852003.
- Thijs RD, Surges R, O’Brien TJ, Sander JW. Epilepsy in adults. Lancet. 2019 Feb 16;393(10172):689-701. doi: 10.1016/S0140-6736(18)32596-0. Epub 2019 Jan 24. PMID: 30686584.

Lo sentimos, el formulario de comentarios está cerrado en este momento.